Součást výstupu V002 v rámci projektu NAZV QF4108
„Využití techniky fúze protoplastů ve šlechtění hospodářsky významných plodin rodu Brassica, Cucumis a Solanum“
uplatněné a ověřené při řešení MSM 6010980701
„Molekulární a technologické základy produkce kvalitních brambor“
Autorský kolektiv:
Ing. Marie Greplová
Mgr. Hana Polzerová
Ing. Jaroslava Domkářová, Ph.D., MBA
1. Úvod
Efektivní tvorba nových odrůd s požadovanými znaky vyžaduje kombinaci tradičních šlechtitelských postupů s moderními technologiemi, jako jsou kultury in vitro, zahrnující produkci dihaploidních linií, fúze protoplastů a využití transformace při vytváření geneticky modifikovaných organismů. Moderní rostlinné biotechnologie se stávají nezbytnou součástí šlechtění rostlin na rezistenci vůči biotickým a abiotickým stresům a přispívají tak k rozšíření odrůdového spektra a ke snížení nákladů na chemické ochranné prostředky. Rezistentní šlechtění (sexuální hybridizace) hospodářsky významných plodin vůči chorobám a abiotickým činitelům často naráží na řadu komplikací jako je sexuální inkompatibilita rodičovských genotypů, nevhodný poměr EBN (Endosperm Balance Number, Carputo a kol. 1997) nebo malá úspěšnost tradiční sexuální hybridizace. Problémy s přenosem rezistence v klasických postupech vedly k výzkumu možnosti netradičních postupů jak u modelových rostlin, tak i u dalších druhů. Alternativní způsob přenosu genů nabízí mezidruhové nebo mezirodové fúze protoplastů (Millam a kol. 1995). Protože neexistují bariéry ve fúzi protoplastů, až dosud inkompatibilní a tedy reprodukčně izolované druhy mohou být kombinovány na úrovni protoplastů. Heterokaryony vzniklé fúzí obsahující jádro dvou druhů ve společné cytoplazmě, regenerují novou buněčnou stěnu, zahajují dělení, při kterém dochází k jaderné fúzi a vzniku somatické hybridní buňky. Somatická hybridní buňka je totipotentní a tedy schopná embryogeneze nebo organogeneze a vývoje v celistvou rostlinu. Materiálem vhodným pro získávání protoplastů jsou kultury in vitro, kde odpadá problematická povrchová sterilizace. Z rostlinných orgánů jsou obecně vhodné a použitelné různé části rostliny, obvykle to jsou buňky listového mezofylu, mladých hypokotylů, popřípadě kalusů. Somatická hybridizace poskytuje nejenom metodu k produkci hybridů mezi sexuálně inkompatibilními druhy, ale i cestu pro genetickou modifikaci vegetativně množených plodin, sterilních nebo částečně fertilních druhů a jedinců s přirozeně dlouhým životním cyklem. Protoplastové fúze a regenerace také umožňují mezidruhový a vnitrodruhový přenos extranukleárních genetických elementů jako je mitochondriální DNA (cytoplasmová samčí sterilita), chloroplasty a cytoplasma. Aplikace somatické fúze vyžaduje nejen regeneraci rostlin z protoplastů, ale i úspěšnou integraci získaných regenerantů do šlechtitelského programu. Somatický hybrid by měl být schopen zpětného křížení s kulturní plodinou k vývoji nové variety. Metoda somatické hybridizace byla již ve světě úspěšně aplikována u celé řady kulturních rostlin včetně rodu Solanum a byl potvrzen přenos rezistence nebo nových kvalitativních znaků (Butenko a kol. 1982, Austin a kol. 1985, Pehu a kol. 1989, Pehu a kol.1990, Schilde-Rentschler a kol. 1993, Thieme a kol. 1997, Helgeson a Haberlach 1999).
V rámci řešení projektu byla propracována metodika izolace protoplastů, fúze protoplastů elektrickým polem a kultivace produktů fúze.
2. Metodický postup
Předkládaný metodický postup fúze protoplastů elektrickým polem vyžaduje dostatek vhodného rostlinného materiálu pro izolaci protoplastů a po vlastní elektrofúzi jejich kultivaci k dosažení regenerace rostlin. Vlastní metodika má tedy čtyři nedílné části.
- Kultivace donorových rostlin
- Izolace protoplastů
- Ověření životnosti protoplastů a fúze protoplastů elektrickým polem
- Kultivace produktů fúze
2.1 Kultivace donorových rostlin
In vitro rostliny pěstujeme v klimatizační komoře s fotoperiodou 16 h/8 h světlo/tma (světelné podmínky: zářivky, typ světla – „daylight“, intenzita - 60 µmol m-2 s-1), při 22 °C. Rostliny kultivujeme na MS mediu bez hormonů (Murashige a Skoog 1962).

Obr. 1 Rostliny rodu Solanum kultivované
in vitro pro izolaci protoplastů
Rostliny určené pro izolaci protoplastů množíme na SH médiu bez hormonů (Schenk a Hildebrand 1972) obohaceném o AgNO3 a Alar 85 (succinic acid dimethylhydrazide) - 10 až 20 rostlin od každého rodičovského genotypu. Rostliny necháme růst po dobu 4 - 6 týdnů (Obr. 1 Rostliny rodu Solanum kultivované in vitro pro izolaci protoplastů). Den před izolací vystavíme rostliny chladu (10 °C) a tmě po dobu 24 hodin. Tyto stresové podmínky umožní synchronizaci buněčného cyklu, což se pozitivně odrazí v následné regeneraci protoplastů.
2.2 Izolace protoplastů
Celý proces izolace protoplastů probíhá ve sterilním prostředí.
Odtrhneme listy (z 10 rostlin, 0,5 - 1 g), rozřežeme je na malé kousky ostrým skalpelem v jedné Petriho misce (Ø = 5 cm) obsahující 5 - 6 ml roztoku enzymu (Bříza a Machová 1991) a utěsníme Petriho misku Parafilmem.
Petriho misky inkubujeme ve tmě přes noc (14 – 16 h) v termostatu při 25 oC; po uplynutí této doby zhodnotíme stav rostlinné tkáně pod mikroskopem; v některých případech (v závislosti na genotypu) umístíme Petriho misky na třepačku asi na15 min.
Rostlinnou tkáň s enzymatickým roztokem přeneseme pomocí jednorázové pipety s otevřeným koncem na sítko (velikost pórů 75 µm) umístěné na Petriho misce (Ø = 5 cm) a za jemného míchání propláchneme sítko sterilním roztokem 0,5 M sacharózy. Tímto krokem oddělíme uvolněné protoplasty od zbytku rostlinné tkáně. Takto získanou suspenzi protoplastů rozdělíme do centrifugačních zkumavek (8 ml) a převrstvíme roztokem W5 (Menczel a kol. 1981) o objemu 1 ml.
Centrifugujeme 12 min při 700 rpm.

Obr. 2 Nepoškozené protoplasty
na rozhraní roztoku sacharózy a W5
Pasteurovou pipetou opatrně odsajeme plující protoplasty tvořící prstýnek (Obr. 2 Nepoškozené protoplasty na rozhraní roztoku sacharózy a W5) na rozhraní použitých roztoků a umístíme je do nové centrifugační zkumavky, přidáme potřebné množství W5 (5 ml) a resuspendujeme.
Centrifugujeme 6 min při 500 rpm.
Pasteurovou pipetou odstraníme supernatant, přidáme W5 (2 – 5 ml) a resuspendujeme pelet.
Centrifugujeme 6 min při 500 rpm a Pasteurovou pipetou odstraníme supernatant.
Přidáme kultivační médium SW11 (Bříza a Machová 1991), aby bylo dosaženo požadované hustoty 6×105/ml (viz 2.3.2) nebo pokračujeme dle protokolu fúze protoplastů elektrickým polem.
2.3 Ověření životnosti, úprava hustoty a fúze protoplastů elektrickým polem
2.3.1 Vyhodnocení životnosti protoplastů před fúzí
20 µl ředěného FDA + 20 µl suspense protoplastů pipetujeme na podložní sklo, vytvoříme preparát. Po 4 - 5 minutách vyhodnotíme preparát pomocí fluorescenčního mikroskopu. Ve vybraném zorném poli bez UV světla spočteme protoplasty a následně zeleně svítící protoplasty v UV světle (zeleně svítící protoplasty jsou živé). Vypočteme procentní podíl životných protoplastů z celkového počtu protoplastů v zorném poli. Při životnosti nad 50 % je zkoumaná suspenze použitelná pro fúze.
2.3.2 Určení hustoty protoplastů pomocí Bürkerovy komůrky
Úprava koncentrace protoplastů před fúzí (před kultivací) probíhá ve sterilním prostředí.
K naizolovaným protoplastům přidáme Pasteurovou pipetou přiměřené množství (2 – 4 ml) předfúzního roztoku (Schilde-Renschler a Ninneman 1988), resuspendujeme (v tomto roztoku mohou protoplasty pobývat až 2 hodiny v lednici při 6 – 7 oC) a určíme hustotu protoplastů pomocí Bürkerovy komůrky.
Zhotovíme preparát, počítáme protoplasty v pěti 3× orámovaných čtvercích (tj. čtverce o straně 1 mm), vlevo a nahoře počítáme všechny buňky dotýkající se střední linky, vpravo a dole tyto nepočítáme. Stanovíme průměrný počet protoplastů z pěti čtverců, což odpovídá hodnotě „X“. Koncentrace buněk v 1 ml pak je: „X“ × 104 (1 čtverec reprezentuje objem 0,1 mm3 tj. 10-4 cm3 [1 cm3 = 1 ml]).
Celkový počet protoplastů z hmoty listů = Vsuspenze × „X“ × 104
Faktor ředění Fř = požadovaná hustota / „X“ × 104
Výsledný objem suspense v požadované hustotě = Vsuspenze / Fř
Následně podle potřeby upravíme koncentraci pro fúze (viz 2.3.3) nebo kultivace protoplastů.
2.3.3 Úprava koncentrace protoplastů před fúzí a fúze protoplastů
Centrifugujeme 3 min při 500 rpm a Pasteurovou pipetou odstraníme supernatant. Celý proces fúze protoplastů probíhá ve sterilním prostředí.
Pasteurovou pipetou přidáme fúzní roztok (Schilde-Renschler a Ninneman 1988), aby byla dosažena požadovaná koncentrace protoplastů pro fúzi 6×105/ml a protoplasty resuspendujeme.
Smícháme suspenze protoplastů dvou fúzních partnerů v poměru 1:1.

Obr. 3 Příklad uspořádání fúzního experimentu
Fúze protoplastů je uskutečněna pomocí elektroporátoru (ECM 2001, BTX, Inc., San Diego, CA) a příslušenství (mikroskop, držák na fúzní komůrky, fúzní komůrky, Obr. 3 Příklad uspořádání fúzního experimentu). Mikroskop umístíme do flowboxu, před fúzí vysterilizujeme komůrky 70% alkoholem a necháme vyschnout. Po vyschnutí naneseme Pasteurovou pipetou 20 - 30 µl suspenze protoplastů do elekroporační komůrky, umístíme do držáku, celý proces fúze sledujeme v invertním mikroskopu.
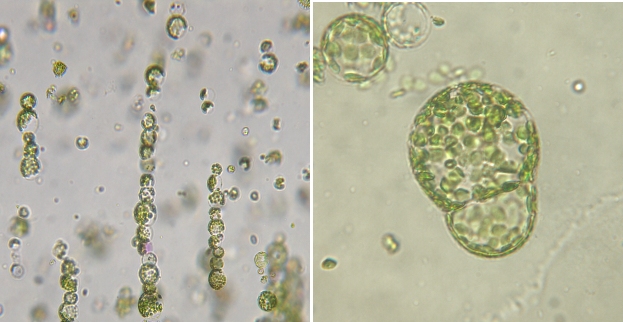
Obr. 4 Příklad fúze protoplastů - vlevo aplikace AC pole, vpravo aplikace DC pulsu
Proces fúze protoplastů: protoplasty se nechají seřadit za působení střídavého proudu (AC field), poté je aplikován puls stejnosměrného proudu (DC pulse), který vede k fúzi (Obr. 4 Příklad fúze protoplastů - vlevo aplikace AC pole, vpravo aplikace DC pulsu).
- Základní parametry elektrického pole
| AC |
5 V/komora se vzdáleností elektrod 0,5 mm |
2 – 18s |
| DC puls |
10 V/ komora se vzdáleností elektrod 0,5 mm |
80 µs |
| AC |
30 V/komora se vzdáleností elektrod 3,2 mm |
2 – 18s |
| DC puls |
60 V/komora se vzdáleností elektrod 3,2 mm |
80 µs |
Po fúzi umístíme protoplasty z pěti komůrek Pasteurovou pipetou do jedné Petriho misky (Ø = 3,5 cm), k suspenzi protoplastů přidáme 1 ml kultivačního média (tekuté SW11, Bříza a Machová 1991). Petriho misky zatěsníme Parafilmem, přemístíme je do termostatu a kultivujeme ve tmě při 25 oC. Další kultivace dle protokolu kultivace produktů fúze protoplastů.
2.4 Kultivace produktů fúze protoplastů
Celý proces kultivace produktů fúze probíhá ve sterilním prostředí.

Obr. 5 Regenerace produktů fúze;
a, b - mikrokalusy v tekutém médiu SW11
c - kalusy v tekutém médiu Shepard D,
d – kalusy na médiu Shepard D zpevněném agarem,
e - regenerace prýtů na kalusech před seříznutím
První buněčné dělení se obvykle uskuteční 2 – 3 dny po fúzi (ověříme pod mikroskopem), po vytvoření buněčné stěny přidáváme v intervalu 7 – 10 dní tekuté médium SW11 se snižující se hladinou osmotika až do stádia mikrokalusů (tj. postupně SW11 0,5M manitol, SW11 0,4 M manitol, SW11 0,3M manitol, Bříza a Machová 1991; Obr. 5 Regenerace produktů fúze; a, b - mikrokalusy v tekutém médiu SW11). Po vytvoření buněčné stěny možno kultivovat na světle (16 h fotoperioda/ 22 oC; světelné podmínky: fluorescenční zářivky – „daylight“, 150 µmol m-2 s-1).
Mikrokalusy se formují 3 – 4 týdny po fúzi, jsou-li již viditelné - provádí se výměna média. Médium SW11 odsajeme a nahradíme tekutým médiem Shepard C (Shepard a Totten 1977). Po 7 – 10 dnech výměnu 2x opakujeme.
Následně sterilně přeneseme kalusy do čistých Petriho misek. Část kalusů kultivujeme v tekutém médiu Shepard D (Shepard a Totten 1977), výměnu média provádíme po 7 – 10 dnech až do regenerace stonků. Část kalusů kultivujeme na agarem zpevněném médiu Shepard D, na kterém se kalusy pasážují po 14 dnech až do regenerace stonků (Obr. 5 Regenerace produktů fúze; c - kalusy v tekutém médiu Shepard D, d – kalusy na médiu Shepard D zpevněném agarem).
První stonky se vyvíjejí 4 – 12 týdnů po zahájení kultivace na médiu Shepard D (Obr. 5 Regenerace produktů fúze; e - regenerace prýtů na kalusech před seříznutím), regenerované prýty seřízneme a necháme zakořenit na MS médiu (Murashige a Skoog 1962). Regeneranty kultivujeme za stejných podmínek jako donorové rostliny pro izolaci protoplastů. Rostliny množíme do dvojic k následnému testování hybridity.
3 Použité roztoky a média – jejich příprava
3.1
- Murashige & Skoog médium
| MS (Duchefa Biochemie) |
4,4 g |
| sacharóza |
30 g |
| agar |
8 g |
MS a sacharózu rozpustíme v 490 ml destilované vody, upravíme pH na 5,6 – 5,8 a doplníme na objem 500 ml destilovanou vodou. Agar rozpustíme v 400 ml destilované vody a rozvaříme v mikrovlnné troubě nebo ve vodní lázni, doplníme na konečný objem (500 ml). Oba roztoky spojíme a promícháme a rozlejeme do kultivačních nádob (do výšky 1 – 2 cm) a zavíčkujeme. Nádoby s médiem sterilizujeme autoklávováním při 121 oC 20 min.
- Schenk & Hildebrand médium
| SH médium (Duchefa Biochemie) |
3,2 g |
| Vitamíny SH (Duchefa Biochemie) |
1,01 g |
| sacharóza |
15 g |
| AgNO3 |
0,003 g |
| Alar |
0,0015 g |
| Agar |
8 g |
Kromě agaru vše rozpustíme v 490 ml destilované vody, upravíme pH na 5,6 – 5,8 a doplníme na objem 500 ml destilovanou vodou. Agar rozpustíme v 400 ml destilované vody a rozvaříme v mikrovlnné troubě nebo ve vodní lázni, doplníme na konečný objem (500 ml). Oba roztoky spojíme a promícháme a rozlejeme do kultivačních nádob (do výšky 1 – 2 cm) a zavíčkujeme. Nádoby s médiem sterilizujeme autoklávováním při 114 oC 20 min.
3.2
- Enzymatický roztok
Zásobní roztok:
| CaCl2.2 H2O |
0,735 g |
| MES |
1,952 g |
| Sacharóza |
171,15 g |
| NAA |
0,005 g (zásobní roztok 100 mg/100 ml, sterilizace filtrací) |
| ZT |
0,002 g (zásobní roztok 50 mg/100 ml, sterilizace filtrací) |
Navážku bez růstových regulátorů rozpustíme v 480 ml destilované vody, upravíme pH na 5,6 – 5,8. Zásobní roztok sterilizujeme v autoklávu při 121 °C 20 min. Po sterilizaci přidáme růstové regulátory a doplníme sterilní destilovanou vodou na 500 ml. Rozdělíme po 50 ml do uzavíratelných nádob. Roztok je možné zamrazit na – 20 oC. (ZT = zeatin; NAA = alpha-naphthylenacetic acid; MES = 2 – (N- morpholino)ethanesulfonic acid).
Příprava enzymů:
| Celuláza Onozuka R-10 (Duchefa Biochemie) |
1 g (respektive 1 U) |
| Macerozym R-10 (Duchefa Biochemie) |
0,2 g (respektive 0.2 U) |
Navážku rozpustíme, upravíme pH na 5,6 – 5,8 a doplníme do 50 ml destilovanou vodou a sterilizujeme filtrací. Případně navážku přepočteme podle „U“ jednotek uvedených na etiketě konkrétního balení enzymu.
Pracovní roztok enzymů:
50 ml enzymů smícháme ve sterilních podmínkách s 50 ml zásobního roztoku (případný přebytek pro uchování zamrazíme na – 20 oC až na 1 měsíc).
- Roztok W5
| NaCl |
9,0 g |
| KCl |
0,8 g |
| CaCl2.2 H2O |
18,4 g |
| Glukóza |
1,0 g |
| Glycin |
1,0 g |
rozpustíme v 990 ml destilované vody, upravíme pH na 5,8 a doplníme destilovanou vodou na 1000 ml. Sterilizujeme v autoklávu při 121 °C 20 min, uchováváme v chladu při 6 – 7 oC.
3.3
3.4
- Médium SW11
| SW11 |
SW11
|
SW11 (0,4M)
|
SW11 ( 0,3M)
|
SW11 ( 0,2M)
|
| |
|
|
|
|
| KNO3 |
950 mg
|
|
|
|
| CaCl2.2 H2O |
367,5 mg
|
|
|
|
| MgSO4. 2 H2O |
185 mg
|
|
|
|
| KH2PO4 |
85 mg
|
|
|
|
| NH4Cl |
133 mg
|
|
|
|
| Myo-inositol |
100 mg
|
|
|
|
| Casein hydrolysate |
500 mg
|
|
|
|
| L-glutamin |
100 mg
|
|
|
|
| Yeast extract |
100 mg
|
|
|
|
| Sacharóza (0,01M) |
3423 mg
|
|
|
|
| manitol |
89,2682 g
|
72,87 g
|
54,65 g
|
36,44 g
|
| |
|
|
|
|
| Thiamine. HCl |
10 mg
|
připravíme zásobní roztoky (100 ml) |
| Pyridoxine. HCl |
1 mg
|
o koncentraci 1 mg/1 ml |
|
| Nicotinic acid |
1 mg
|
|
|
|
| H3BO3 |
3 mg
|
(a do média pipetujeme příslušné množství, |
| MnSO4. 4H2O |
14 mg
|
např. Thiamine. HCl 10 ml) |
| ZnSO4. 7H2O |
2 mg
|
|
|
|
| CuSO4.5H2O |
0,025 mg
|
|
|
|
| KI |
0,75 mg
|
|
|
|
| Na2MoO4. 2H2O |
0,25 mg
|
|
|
|
| CoCl2. 6H2O |
0,025 mg
|
|
|
|
| FeSO4. 7H2O |
13,9 mg
|
|
|
|
| Na2EDTA.2H2O Chelaton III |
37,3 mg
|
|
|
|
| |
|
|
|
|
| NAA |
2 mg*
|
|
|
|
| 2,4 D |
0,2 mg
|
|
|
|
| Zeatin |
0,5 mg*
|
|
|
|
rozpustíme v 950 ml destilované vody, upravíme pH na 5,6 – 5,8 a sterilizujeme v autoklávu při 121 °C 20 min. Sterilně přidáme Zeatin a NAA a doplníme sterilizovanou destilovanou vodou na 1000 ml, uchováváme v chladu při 6 – 7 oC.
* Zeatin - zásobní roztok 50 mg/ 100ml sterilizujeme filtrací. NAA - zásobní roztok 100 mg/100 ml sterilizujeme filtrací.
- Médium Shepard C a Shepard D
| |
C0,3M
|
C0,2M
|
D0,2M
|
|
| NH4 NO3 |
|
|
1650 mg
|
|
| KNO3 |
1900 mg
|
|
1900 mg
|
|
| CaCl2.2 H2O |
440 mg
|
|
440 mg
|
|
| MgSO4. 7 H2O |
370 mg
|
|
370 mg
|
|
| KH2PO4 |
170 mg
|
|
170 mg
|
|
| Na2EDTA |
37,3 mg
|
|
37,3 mg
|
|
| FeSO4. 7H2O |
27,8 mg
|
|
27,8 mg
|
|
| H3BO3 |
6,2 mg
|
|
6,2 mg
|
připravíme zásobní roztoky (100 ml) |
| MnCl2. 4H2O |
19,8 mg
|
|
19,8 mg
|
o koncentraci 1 mg/1 ml |
| ZnSO4. 7H2O |
9,2 mg
|
|
9,2 mg
|
|
| KI |
0,83 mg
|
|
0,83 mg
|
(a do média pipetujeme příslušné množství, |
| Na2MoO4. 2H2O |
0,25 mg
|
|
0,25 mg
|
např. H3BO3 6,2 ml) |
| CuSO4. 5H2O |
0,025 mg
|
|
0,025 mg
|
|
| CoSO4.7H2O |
0,03 mg
|
|
0,03 mg
|
|
| Myo-inositol |
100 mg
|
|
100 mg
|
|
| Thiamin. HCl |
0,5 mg
|
|
0,5 mg
|
|
| Glycin |
2 mg
|
|
2 mg
|
|
| Nicotinic acid |
5 mg
|
|
5 mg
|
|
| Pyridoxine. HCl |
0,5 mg
|
|
0,5 mg
|
|
| Folic acid |
0,5 mg
|
|
0,5 mg
|
|
| Biotin |
0,05 mg
|
|
0,05 mg
|
|
| Casein hydrolyzate |
1000 mg
|
|
1000 mg
|
|
| Adenin sulfát |
40 mg
|
|
40 mg
|
|
| NAA |
0,05 mg*
|
|
|
|
| IAA |
|
|
0,1 mg*
|
|
| BAP (6-benzylaminopurin) |
0,5 mg*
|
|
|
|
| Zeatin |
|
|
0,5 mg*
|
|
| Manitol |
54,654 g
|
36,44 g
|
36,44 g
|
|
| Sacharóza 15 mM |
5,1345 g
|
|
5,1345 g
|
|
| MES |
0,976 g
|
|
0,976 g
|
|
| Agar (zpevněné médium) |
|
|
7 g
|
|
rozpustíme v 950 ml destilované vody, upravíme pH na 5,8 a sterilizujeme v autoklávu při 121 °C 20 min. Sterilně přidáme NAA, IAA, zeatin, BAP popř. kyselinu giberelovou (viz výše) a doplníme sterilizovanou destilovanou vodou na 1000 ml, uchováváme v chladu. Shepard D připravujeme buď tekuté médium nebo s agarem, agarem zpevněné médium rozléváme do Petriho misek ve flow-boxu.
* Zeatin - zásobní roztok 50 mg/100 ml sterilizujeme filtrací. NAA - zásobní roztok 100 mg/100 ml sterilizujeme filtrací. BAP – zásobní roztok 50 mg/100 ml sterilizujeme filtrací.
3.5 Kontrola sterility použitých roztoků
Všechny roztoky před každým použitím zkontrolujeme bakteriálním testem: 1 ml roztoku + 1 ml provokačního média. Kultivujeme ve tmě při 25 oC po 3 – 4 dnech hodnotíme (přítomnost infekce je indikována mléčným zabarvením roztoku).
Provokační médium: Standard I nutrient broth for microbiology (Merck) – 25 g/l
4 Hodnocení regenerantů
Hybridnost regenerantů je třeba ověřit. Pro hodnocení hybridnosti je vhodné použít k určení ploidie průtokovou cytometrii jako preselekční metodu (http://lmcc.ieb.cz/book/flow-cytometry). Potenciální somatické hybridy je třeba ověřit některou z metod DNA analýzy např. RAPD (Greplová a kol. 2007).
5 Literatura
- Austin S, Baer MA, Helgeson JP (1985) Transfer of resistance to potato leaf roll virus from Solanum brevidens into solanum tuberosum by somatic fusion. Plant Sci 39: 75-82
- Bříza J, Machová I (1991) Regeneration of plants from leaf mesophyll protoplasts of the tetraploid potato cultivars Xenia and Bintje. Biologia plantarum 33 (3): 225-233
- Butenko R, Kuchko A, Komarnitsky I (1982) Some features of somatic hybrids between Solanum tuberosum and S. chacoense and its F1 sexual progeny. In: A. Fujiwara (Ed.), Plant tissue culture. Proc 5th Int Congr Plant Tiss Cell Cult, Tokyo: 643-644
- Carputo D, Barone A, Cardi T, Sebastano A, Frusciante L, Peloquin SJ (1997) Endosperm balance number manipulation for direct in vivo germplasm introgression to potato from a sexually isolated relative (Solanum commersonii Dun.). Proceedings of the National Academy of Sciences of the United States of America 94 (22): 12013-12017
- Helgeson JP, Haberlach GT (1999) Somatic hybrids of Solanum tuberosum and related specie. In: Plant biotechnology and in vitro biology in the 21st century (Eds Altman A, Ziv M, Izhar S) Kluwer Academic Publishers, Dordrecht: 151-154
- Greplová M, Polzerová H, Kreuz L (2007) Protoplast fusion by electric field at the model material S. tuberosum L. Scientific studies 15 – Potato Research Institute Havlíčkův Brod, 2007: 71-83
- Menczel L, Nagy F, Kiss ZR, Maliga P (1981) Streptomycin resistant and sensitive somatic hybrids of Nicotiana tabacum + Nicotiana knightiana: correlation of resistance to N. tabacum plastids. Theor Appl Genet 59: 191-195
- Millam S, Payne LA, Mackay GR (1995) The integration of protoplast fusion-derived material into a potato breeding programme – a review of progress and problems. Euphytica 85: 451-455
- Murashige T, Skoog F (1962) A revised medium for rapid growth and bioassays with tobacco tissue culture. Physiol Plant 15: 473-497
- Pehu E, Karp A, Moore K Steele S, Dunckley R, Jones MG K (1989) Molecular, cytogenetic and morphological characterization of somatic hybrids of dihaploid Solanum tuberosum and diploid S. brevidens. Theor Appl Genet 78: 696-704
- Pehu E, Gibson RW, Jones MG K, Karp A (1990) Studies on the genetic basis of resistance to Potato Leaf Roll Virus, Potato Virus Y and Potato Virus X in Solanum brevidens using somatic hybrids of Solanum brevidens and Solanum tuberosum. Plant Sci 69: 95-101
- Schenk RU, Hildebrandt AC (1972) Medium and techniques for induction and growth of monocotyledonous and dicotyledonous plant cell cultures. Can J Bot 50: 199-204
- Shepard FJ, Totten RE (1977) Messophyll cell protoplasts of potato. Plant Physiol 60: 313-316
- Simko I (2002) Comparative analysis of quantitative trait loci for foliage resistance to Phytophthora infestans in tuber-bearing Solanum species. Amer J Potato Res 79: 125-132
- Schilde-Renschler L, Ninnemann H (1988) Kombination von Kartoffellinien durch Protoplastenfusion zur Regeneration tetraploider züchterisch nutzbarer Hybidpflanzen. Vortr Pflanzenzüchtg 14: 149-163
- Schilde-Rentschler L, Ruoss B, Schierbaum B, Ninnemann H (1993) Availability of new genetic resources from wild species for potato breeding. Abstracts 12 th triennal EAPR conference Paris: 99-100
- Thieme R, Darsow U, Gavrilenko T, Dorokhov D, Tiemann H (1997) Production of somatic hybrids between S. tuberosum L. and late blight resistant Mexican wild potato species. Euphytica 97: 189-200
Poděkování
Autoři děkují recenzentovi Doc. Ing. Josefu Habětínkovi, CSc. za prostudování rukopisu a cenné připomínky.